Những câu hỏi liên quan
32. Cho hợp chất hữu cơ A có thành phần % khối lượng các nguyên tố.lần lượt là C(40%) , H(6,67%) , O(53,33%). Biết khi hoá hơi hoàn toàn 12g Z thì thu đc thể tích hơi bằng thể tích của 14,2g khí Clo ( khi xét cùng điều kiện) . CTPT của Z?
Xem chi tiết
\(M_Z = \dfrac{12}{\dfrac{14,2}{71}} = 60(đvC)\)
Số nguyên tử Cacbon = \(\dfrac{60.40\%}{12} = 2\)
Số nguyên tử Hidro = \(\dfrac{60.6,67\%}{1} = 4\)
Số nguyên tử Oxi = \(\dfrac{60.53,33\%}{16} = 2\)
Vậy CTPT của Z : C2H4O2
Đúng 2
Bình luận (0)
21. Khi hoá hơi hoàn toàn 4,6g hợp chất hữu cơ X thì thu đc thể tích hơi đúng bằng thể tích của 2,8g khí nito ở cùng điều kiện. Khối lượng mol của X là?
Xem chi tiết
nN2 = \(\dfrac{2,8}{28}\)= 0,1 mol
4,6 gam X có thể tích bằng thể tích 2,8 gam nito => số mol của 4,6 gam X = số mol 2,8 gam nito = 0,1 mol
=> MX = \(\dfrac{4,6}{0,1}\) = 46 (g/mol)
Đúng 1
Bình luận (0)
35. Một hợp chất hữu cơ B có thành phần % khối lượng C,H,O lần lượt là: 48,65% , 8,11% và 43,24%. Biết rằng , cùng 1 thể tích hơi ( khi xét cùng đk) thì chất B nặng hơn khí oxi 2,3125 lần. CTPT của B là?
Xem chi tiết
Gọi công thức đơn giản nhất là CxHyOz
%mO = 100% - %mC - %mH = 43,24%
Ta có:
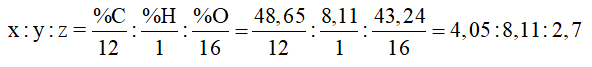
=> x : y : z = 1,5 : 3 : 1 = 3 : 6 : 2
=> CTĐGN của A là C3H6O2
=> CTPT của A dạng (C3H6O2)n
MA = 74 = (12.3 + 6 + 16.2).n => n = 1
=> CTPT: C3H6O2
Đúng 2
Bình luận (0)
Anh chị làm ơn giúp e mấy bài này ạ.E cảm ơn!Bài 1:Khi đốt cháy hoàn toàn một lượng hợp chất hữu cơ X cần 0,8 gam O2 người ta thu được 1,1 gam CO2,0,45 gam H2O và không có sản phẩm nào khác. Xác định công thức phân tử của X. Biết rằng khi cho bay hơi hoàn toàn 0,6gam X ở điều kiện nhiệt độ và áp suất thích hợp đã thu được một thể tích hơi đúng bằng thể tích hơi của 0,32 gam O2 trong cùng điều kiện.Bài 2:Đốt cháy hoàn toàn một hợp chất hữu cơ A có thành phần C,H,O thu được CO2 có thể tích bằng 3/...
Đọc tiếp
Anh chị làm ơn giúp e mấy bài này ạ.E cảm ơn!
Bài 1:
Khi đốt cháy hoàn toàn một lượng hợp chất hữu cơ X cần 0,8 gam O2 người ta thu được 1,1 gam CO2,0,45 gam H2O và không có sản phẩm nào khác. Xác định công thức phân tử của X. Biết rằng khi cho bay hơi hoàn toàn 0,6gam X ở điều kiện nhiệt độ và áp suất thích hợp đã thu được một thể tích hơi đúng bằng thể tích hơi của 0,32 gam O2 trong cùng điều kiện.
Bài 2:
Đốt cháy hoàn toàn một hợp chất hữu cơ A có thành phần C,H,O thu được CO2 có thể tích bằng 3/4 thể tích hơi nước và bằng 6/7 thể tích O2 dùng để đốt cháy. Mặt khác, 1l hơi A có khối lượng bằng 46 lần khối lượng 1 lít H2 ở cùng điều kiện.Tìm công thức phân tử của A.
Bài 3: Đốt cháy hoàn toàn 4,3 gam hợp chất hữu cơ thu được 6,72 lít CO2 và 0,35 mol H2O. Khi đốt cháy hoàn toàn 1 mol chất A cần 212,8l O2.Xác định CTPT của A.
6. Oxi hoá hoàn toàn 14,75g một hợp chất hữu cơ X bằng CuO dư , đun nóng , thu được 16,80 lít CO2 ; 2,80 lít N2 ( các thể tích đo ở đktc) và 20,25g H2O. Thành phần % về khối lượng các nguyên tố C,H,N có trong X lần lượt là?
Xem chi tiết
Khi đốt cháy hoàn toàn 5,9 gam hợp chất hữu cơ A thu được 6,72 lít khí CO2(đkc); 1,12 lít khí N2 và 8,1g H2O. Mặt khác, khi hoá hơi 2,9 gam hợp chất hữu cơ A chiếm thể tích đúng bằng thể tích của 1,6g O2 ở cùng điều kiện. Tìm công thức phân tử hợp chất hữu cơ A.
Khi phân tích một hợp chất hữu cơ (X) có thành phần như sau: %C 52,17%; %H 13,04% và %O 34,78%. Công thức phân tử của (X) nào sau đây đúng ? Biết công thức đơn giản nhất trùng với công thức phân tử A. C2H6O B. CH4O C. C3H8O D. C4H10O
Đọc tiếp
Khi phân tích một hợp chất hữu cơ (X) có thành phần như sau: %C = 52,17%; %H = 13,04% và %O = 34,78%. Công thức phân tử của (X) nào sau đây đúng ? Biết công thức đơn giản nhất trùng với công thức phân tử
A. C2H6O
B. CH4O
C. C3H8O
D. C4H10O
Đốt cháy hoàn toàn 1,72 gam chất hữu cơ (E) thu được 3,52 gam CO2; 1,80 gam H2O và một lượng khí N2. Tìm công thức phân tử của E. biết khi hoá hơi 1,29 gam E thì thu được thể tích hơi đúng bằng thể tích 0,96 gam oxi trong cùng điều kiện
\(n_{CO_2}=\dfrac{3.52}{44}=0.08\left(mol\right)\)
\(n_{H_2O}=\dfrac{1.8}{18}=0.1\left(mol\right)\)
\(m_N=1.72-0.08\cdot12-0.1\cdot2=0.56\left(g\right)\)
\(n_N=\dfrac{0.56}{14}=0.04\left(mol\right)\)
\(M_E=\dfrac{1.29}{\dfrac{0.96}{32}}=43\left(đvc\right)\)
\(n_E=\dfrac{1.72}{43}=0.04\left(mol\right)\)
Số nguyên tử C : \(\dfrac{0.08}{0.04}=2\)
Số nguyên tử H : \(\dfrac{0.2}{0.04}=5\)
Số nguyên tử N : \(\dfrac{0.04}{0.04}=1\)
\(CT:C_2H_5N\)
Đúng 1
Bình luận (0)
Hỗn hợp M ở thể lỏng, chứa hai hợp chất hữu cơ kế tiếp nhau trong một dãy đồng đẳng. Nếu làm bay hơi 2,58 g M thì thể tích hơi thu được đúng bằng thể tích của 1,40 g khí
N
2
ở cùng điều kiện.Đốt cháy hoàn toàn 6,45 g M thì thu được 7,65 g
H
2
O
và 6,72 lít
C
O
2
(đktc).Xác định công thức phân tử và phần trăm khối lượng của từng chất trong hỗn hợp...
Đọc tiếp
Hỗn hợp M ở thể lỏng, chứa hai hợp chất hữu cơ kế tiếp nhau trong một dãy đồng đẳng. Nếu làm bay hơi 2,58 g M thì thể tích hơi thu được đúng bằng thể tích của 1,40 g khí N 2 ở cùng điều kiện.
Đốt cháy hoàn toàn 6,45 g M thì thu được 7,65 g H 2 O và 6,72 lít C O 2 (đktc).
Xác định công thức phân tử và phần trăm khối lượng của từng chất trong hỗn hợp M.
Số mol 2 chất trong 2,58 g M: 
Số mol 2 chất trong 6,45 g M: 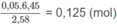
Khi đốt hỗn hợp M, thu được C O 2 và H 2 O ; vậy các chất trong hỗn hợp phải chứa C và H, có thể có O. Hai chất lại kế tiếp nhau trong một dãy đồng đẳng (nghĩa là hom nhau 1 nhóm CH2) nên công thức phân tử hai chất đó là C x H y O z và C x + 1 H y + 2 O z (x, y nguyên và > 0; z nguyên và > 0).
Giả sử trong 6,45 g M có a moi C x H y O z và b mol C x + 1 H y + 2 O z :
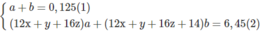
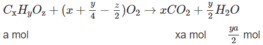
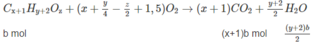
Số mol C O 2 :
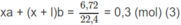
Số mol H 2 O :
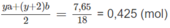
⇒ ya + (y + 2)b = 0,85 (4)
Giải hệ phương trình :
Biến đổi (3) ta có x(a + b) + b = 0,300
b = 0,300-0,125x
0 < b < 0,125 ⇒ 0 < 0,300 - 0,125x < 0,125
1,40 < x < 2,40
⇒ x = 2; b = 0,300 - 0,125.2 = 0,05.
⇒ a = 0,125 - 0,05 = 0,075.
Thay giá trị của a và b vào (4) ta có :
0,0750y + 0,0500(y + 2) = 0,85
⇒ y = 6.
Thay giá trị của a, b, x, y vào (2) ta tìm được z = 1.
Thành phần hỗn hợp M :
Khối lượng
C
2
H
6
O
chiếm 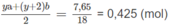
Khối lượng
C
3
H
g
O
chiếm 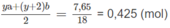
Đúng 0
Bình luận (0)